Anvisa aprimora rotulagem de medicamentos
A Diretoria Colegiada (Dicol) da Anvisa aprovou, na sua 11ª Reunião Ordinária Pública, um conjunto de alterações pontuais na Resolução da Diretoria Colegiada (RDC) 768, de 12 de dezembro de 2022, que estabelece as regras para a rotulagem de medicamentos, com o intuito de aprimorar o marco regulatório existente.
As alterações preservam o objetivo desse marco regulatório para a segurança do paciente e o uso correto dos medicamentos, garantindo o acesso às informações das embalagens de forma clara e inequívoca.
Nesse sentido, para algumas informações necessárias ao autocuidado do paciente, quando da aquisição e uso de um medicamento isento de prescrição, como por exemplo a indicação e a classe terapêutica de um produto, a alteração aprovada passou a permitir sua colocação na face frontal da embalagem, facilitando assim a sua visualização.
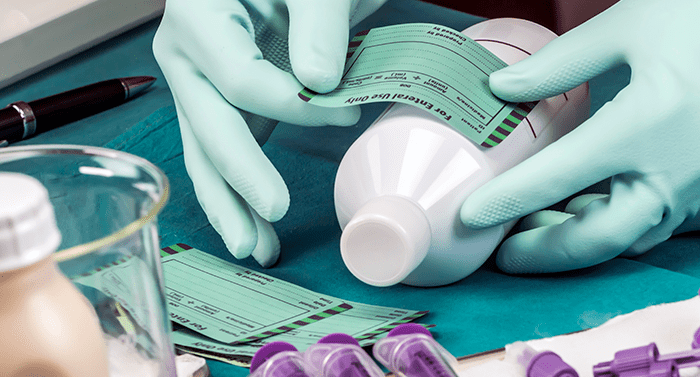
Dentre as principais mudanças trazidas pelos normativos, destaca-se a proibição da gravação de informações diretamente nas ampolas, frascos-ampola e seringas de vidro ou outro recipiente de embalagem de soluções parenterais de pequeno volume (SPPV), que são soluções estéreis destinadas à administração parenteral, acondicionadas em recipiente com capacidade inferior a 100 ml. Em substituição, a norma prevê a utilização de etiquetas adesivas indeléveis, que permitem o contraste de cores nos rótulos desses produtos, melhorando a visualização e diferenciação de informações essenciais, com vistas a mitigar a ocorrência de erros de medicação e, consequentemente, vários eventos adversos aos usuários, que poderiam inclusive levar a óbitos.
Outro importante avanço das normas é a adoção da técnica “Tall Man Lettering”, mecanismo capaz de diferenciar nomes de princípios ativos que possuem similaridade fonética ou gráfica, por meio do uso de letras maiúsculas e em negrito que ajudam a diferenciar nomes de medicamentos semelhantes. Medicamentos destinados ou de uso restrito a estabelecimentos de saúde são aqueles utilizados em hospitais, clínicas, ambulatórios, serviços de atenção domiciliar e outros estabelecimentos de assistência à saúde.
A técnica de TML é uma das ferramentas utilizadas para ajudar a minimizar os erros de medicações decorridos da troca acidental entre princípios ativos com fonética e/ou ortografia semelhantes, pois consiste em escrever em negrito e em letras maiúsculas a parte diferente do nome dos medicamentos que apresentam essas semelhanças no som e/ou grafia.
Com objetivo semelhante, foi permitida a colocação da quantidade total do medicamento na face frontal da embalagem. Isso auxilia o cidadão na comparação de preço dos produtos, sem, no entanto, causar prejuízo para a compreensão das informações relacionadas ao uso seguro do medicamento.
Para os medicamentos com destinação governamental, ou seja, aqueles embalados para serem vendidos ao Governo Federal, foi autorizado que as frases “VENDA SOB PRESCRIÇÃO” e “VENDA SOB PRESCRIÇÃO COM RETENÇÃO DA RECEITA” sejam substituídas pelas frases “USO SOB PRESCRIÇÃO” e “USO SOB PRESCRIÇÃO E RETENÇÃO DA RECEITA”. Além disso, a utilização dessas frases passa a ser obrigatória somente na embalagem secundária do medicamento, considerando-se que tal alteração não trará prejuízo à disposição dos elementos da rotulagem relacionados ao uso seguro dos medicamentos.
Foram publicadas pela Anvisa 5 novas normas:
- Resolução da Diretoria Colegiada – RDC nº 768, de 12 de dezembro de 2022, que estabelece as regras para a rotulagem de medicamentos, definindo os critérios, aprimorando a forma e o conteúdo dos dizeres de rotulagem de todos os medicamentos regularizados no Brasil;
- Instrução Normativa – IN nº 198, de 12 de dezembro de 2022, que estabelece requerimentos específicos para a rotulagem de soluções parenterais de grande volume, soluções para irrigação, diálise, expansores plasmáticos e soluções parenterais de pequeno volume;
- Instrução Normativa – IN nº 199, de 12 de dezembro de 2022, que estabelece a lista dos insumos farmacêuticos ativos com similaridade fonética ou gráfica com outros insumos;
- Resolução da Diretoria Colegiada – RDC nº 770, de 12 de dezembro de 2022, que estabelece frases de alerta em bulas e em embalagens de medicamentos de acordo com as substâncias, classes terapêuticas e listas de controle dos medicamentos;
- Instrução Normativa – IN nº 200, de 12 de dezembro de 2022, que estabelece as substâncias, classes terapêuticas e listas de controle que necessitam de frases de alerta quando presentes em medicamentos, sejam como princípio ativo ou excipiente, e suas respectivas frases;